
搜索网站、位置和人员

新闻活动 新闻动态
近日,西湖大学化学系王怀民团队和浙江大学化学系黄飞鹤团队合作在Nano Letters发表了题为"Controlling Intracellular Enzymatic Self-Assembly of Peptide by Host-Guest Complexation for Programming Cancer Cell Death"的研究论文。该工作提出一种新型多肽组装动力学控制策略,引起细胞内系列“蝴蝶效应”,从而控制特定细胞活性。他们通过引入主客体相互作用力,控制多肽分子在细胞内的酶促组装动力学,实现了功能多肽分子在线粒体内的可控自组装,并引起细胞铁死亡。该工作为多肽组装在细胞内可控编程提供了一种简单易行的方法。

图1. Nano Letters封面图片
癌症是世界范围内主要的公共健康问题之一,临床上主要是通过手术切除癌变组织、放疗、化疗以及免疫治疗来缓解癌症症状,但是放化疗药物的溶解性差,毒副作用大,会对健康细胞进行无差别杀伤,药物的频繁使用也会引起肿瘤细胞的耐药性。而免疫治疗响应率低,个体差异大。因此,开发新的策略对于肿瘤治疗具有重要意义。随着生物材料的发展,基于酶诱导的多肽自组装已经被应用于癌症治疗,然而,多肽的组装速率对其生物活性具有显著的影响。那么,如何控制多肽分子在特定细胞器内发生自组装?如何调控细胞内的酶促组装动力学?
西湖大学王怀民课题组在多肽组装领域进行了多年研究,浙江大学黄飞鹤教授长期从事主客体相互作用的研究。他们经过长期的讨论研究,在多肽自组装体系中引入主客体相互作用,构建了肿瘤细胞内酶促组装动力学可控的小分子多肽自组装体系,实现选择性杀死癌细胞的目的。一方面,主客体复合物的形成可以在不降低多肽组装能力的条件下控制酶反应速度,增强细胞摄取;另一方面,其pH响应特性可使得酶促自组装在细胞膜和线粒体中“缓慢”和“快速”进行,提高多肽在线粒体的局部组装浓度,进而增加肿瘤治疗的靶向性和疗效。
如下图所示,研究团队通过合理设计,合成了具备靶向肿瘤细胞线粒体的多肽分子Fc-TPP1,该分子由四部分组成:自组装疏水多肽片段、肿瘤细胞选择性官能团、靶向线粒体的基团、以及可以发生主客体识别的封端官能团,为了对多肽分子的酶促组装动力学进行调控,作者将水溶性柱[6]芳烃(WP6)引入组装体系中。合成的小分子多肽在体外中性条件下可以与亲水性的WP6通过主客体相互作用形成复合物,使得多肽分子的酶解速率大大降低。而当复合物进入细胞后,在溶酶体的酸性环境作用下,主客体复合物发生破坏,在靶向线粒体基团的作用下,多肽自组装前体分子逃逸出溶酶体,靶向线粒体进行原位自组装,破坏细胞线粒体,引起细胞铁死亡,从而达到杀死癌细胞的目的(图2)。
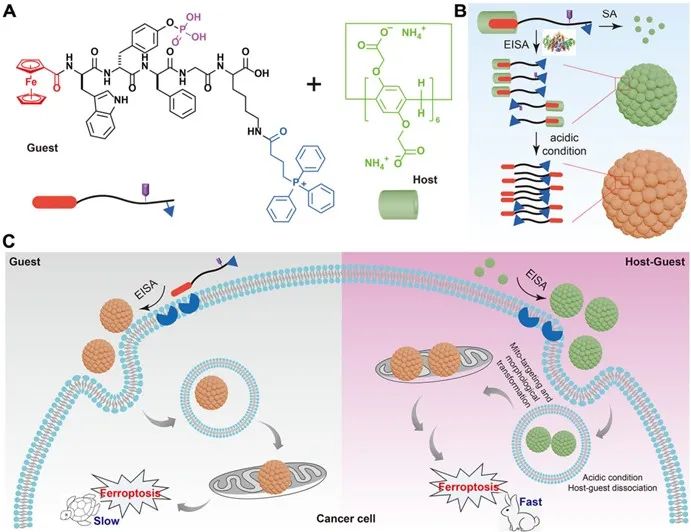
图2. A) 多肽分子Fc-TPP1和WP6的化学结构式;Fc-TPP1与WP6在 B) 体外和 C) 癌细胞内发生可控的酶促自组装,引起癌细胞铁死亡
首先,作者在体外验证了Fc-TPP1与WP6之间的主客体相互作用,确定了Fc-TPP1与WP6之间的结合常数为39.9 μM,结合比为1:1。当在体系中加入碱性磷酸酶(ALP)后,主客体复合物会由聚集的纳米颗粒转变为均一的纳米球结构。通过调节Fc-TPP1与WP6之间的比例,纳米球的粒径可以被精确调控。
将Fc-TPP1/WP6复合物和Fc-TPP1分别与过量表达ALP的人成骨肉瘤细胞(Saos-2)和宫颈癌细胞(HeLa)共孵育,细胞毒性实验表明,经主客体相互作用处理后的Fc-TPP1表现出更大的细胞毒性。对细胞裂解液进行分析,发现Saos-2细胞对经WP6保护后的Fc-TPP1的摄取能力大大提高。激光共聚焦显微镜(CLSM)观察发现,Fc-TPP1/WP6会在细胞线粒体中聚集,并会破坏线粒体(图2A)。进一步分析表明,与主客体复合物孵育后,线粒体的膜电位下降(图2B),细胞产生过量ROS(图2C),肿瘤细胞发生铁死亡。随后,生物电镜(Bio-TEM)结果表明,Saos-2细胞经Fc-TPP1/WP6主客体复合物处理0.5 h后,线粒体内会出现密集的组装体,24 h后,线粒体遭受到破坏,细胞内细胞器的数量减少,并引起其它细胞器的损坏(图2D)。对细胞切片进行光电子能谱(XPS)分析发现,经Fc-TPP1/WP6处理后的细胞具备最高的Fe含量,表明经主客体相互作用保护后的Fc-TPP1可以在肿瘤细胞内发生聚集,组装,并最终引起癌细胞死亡。进一步,将Fc-TPP1/WP6复合物注射到荷瘤小鼠中,可以成功实现对肿瘤的抑制。
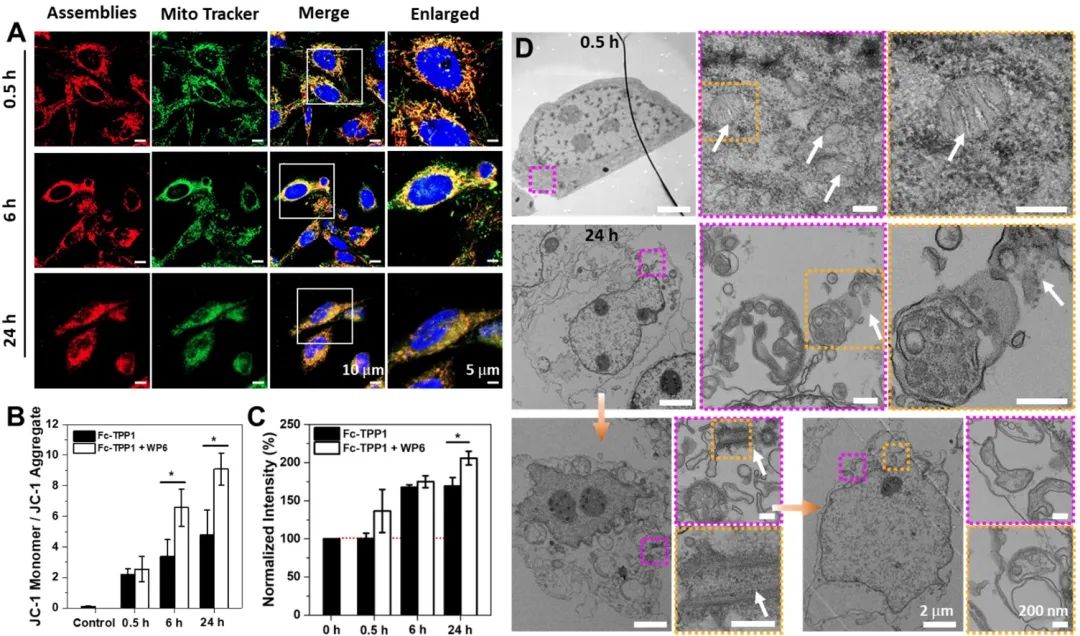
图3. A) Saos-2细胞与Fc-TPP1/WP6孵育0.5h、6h和24h的CLSM图片;经Fc-TPP1和Fc-TPP1/WP6处理后的Saos-2细胞的 B) 细胞膜电位变化以及 C) ROS产生量;D) Saos-2细胞与Fc-TPP1/WP6孵育0.5h和24h的Bio-TEM图片
该工作提出了通过控制细胞内酶促组装动力学的方法对多肽分子在细胞内的组装行为进行调控,精确控制其酶促自组装行为在肿瘤细胞的细胞膜表面和线粒体内分别“缓慢”和“快速”进行,提高了多肽分子的水溶性、细胞摄取能力、以及肿瘤治疗的靶向性,为多肽在细胞内可控编程提供了一种新型策略。该工作受到国家自然科学基金会(82022038,22035006),西湖教育基金会,以及浙江省自然科学基金(LD21B020001)的资助。同时该工作感谢西湖大学分子科学公共实验平台、物质科学公共实验平台以及生物医学实验技术中心在测试方面的协助。
论文信息
Controlling Intracellular Enzymatic Self-Assembly of Peptide by Host-Guest Complexation for Programming Cancer Cell Death
Xuejiao Yang, Bihan Wu, Jiong Zhou, Honglei Lu, Hongyue Zhang, Feihe Huang, and Huaimin Wang*
Nano Letters
智能生物材料实验室介绍
联系方式:wanghuaimin@westlake.edu.cn

















